3.2.1 Heat of Reaction (M)
Quiz Summary
0 of 7 Questions completed
Questions:
Information
You have already completed the quiz before. Hence you can not start it again.
Quiz is loading…
You must sign in or sign up to start the quiz.
You must first complete the following:
Results
Results
0 of 7 Questions answered correctly
Your time:
Time has elapsed
You have reached 0 of 0 point(s), (0)
Earned Point(s): 0 of 0, (0)
0 Essay(s) Pending (Possible Point(s): 0)
Categories
- Not categorized 0%
| Pos. | Name | Entered on | Points | Result |
|---|---|---|---|---|
| Table is loading | ||||
| No data available | ||||
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- Current
- Review
- Answered
- Correct
- Incorrect
-
Question 1 of 7
1. Question
1 point(s)Di bawah ini adalah persamaan termokimia.
2Na + 2H₂O → 2NaOH + H₂ ∆H = -x kJ/mol
Apakah jumlah haba yang dilepaskan jika 0.5 mol natrium bertindak balas dengan air yang mencukupi?
CorrectIncorrect -
Question 2 of 7
2. Question
1 point(s)Persamaan termokimia berikut mewakili pembentukan gas ammonia.
2N₂ + 3H₂ → 2NH₃ ∆H = -xkJ/mol
Yang manakah antara pernyataan berikut adalah benar bagi tindak balas ini?
CorrectIncorrect -
Question 3 of 7
3. Question
1 point(s)C + O₂ → CO₂ ∆H = -394 kJ mol⁻¹
Persamaan di atas mewakili tindak balas pembentukan karbon dioksida. Cari haba yang dilepaskan apabila 6g karbon habis terbakar sepenuhnya dalam oksigen. [Jisim atom relatif karbon = 12]
CorrectIncorrect -
Question 4 of 7
4. Question
1 point(s)Apabila 500 cm³ asid hidroklorik 2.0 mol dm-3 bertindak balas dengan 500 cm³ larutan kalium hidrogen karbonat 2.0 mol dm-3 suhu menurun sebanyak yoC. Apakah pengurangan suhu bagi tindak balas apabila 50 cm³ asid hidroklorik 2.0 mol dm-3 bertindak balas dengan 50 cm³ larutan kalium hidrogen karbonat 2.0 mol dm-3?
CorrectIncorrect -
Question 5 of 7
5. Question
1 point(s)Tindak balas antara 100 cm³ asid hidroklorik 2.0 mol/dm³ dan 100 cm³ larutan natrium hidroksida 2.0 mol/dm³ melepaskan 10 kJ haba. Cari perubahan suhu campuran selepas tindak balas. [Muatan haba tentu larutan = 4.2J g⁻¹; Ketumpatan larutan = 1g/cm³]
CorrectIncorrect -
Question 6 of 7
6. Question
1 point(s)C + O₂ → CO₂ ∆H = -393.5 kJ mol⁻¹
Persamaan di atas mewakili tindak balas pembentukan karbon dioksida. Cari haba yang dilepaskan apabila terbentuk 0.2 mol karbon dioksida.
CorrectIncorrect -
Question 7 of 7
7. Question
1 point(s)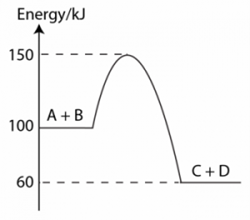
Rajah di atas menunjukkan gambarajah tahap tenaga yang mewakili tindak balas kimia berikut.
A + B → C + D; ∆H = x kJ/mol Apakah nilai x?
CorrectIncorrect