Konsep pH
- Skala pH ialah sekala nombor yang digunakan untuk mengukur keasidan atau kealkaliansuatu larutan akueus berdasarkan kepekatan ion hidrogen H+ dalam akueus itu.
- Mengikut takrifan:
\[pH = – \log [{H^ + }]\]
dan [ H+ ] mewakili kepekatan ion H+ dalam larutan akueus itu. - Ini bermakna pH larutan akueus akan turun apabila kepekatan ion H+ meningkat.
- Semakin tinggi kepekatan ion hidrogen dalam suatu larutan semakin kecil nilai pH larutan asid itu.
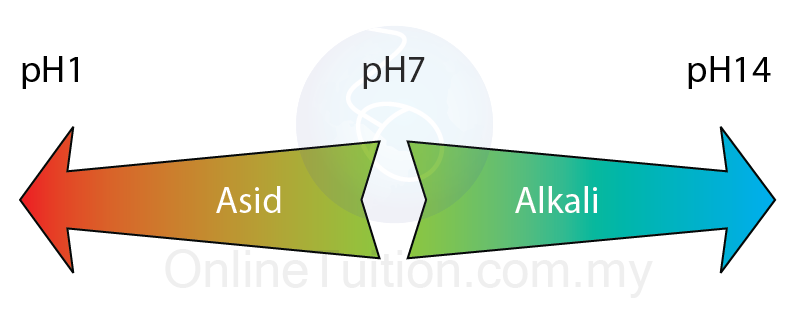
- Nilai pH larutan berasid adalah kurang daripada tujuh. Semakin kecil nilai pH larutan, semakin tinggi keasidannya.
- Nilai pH bagi larutan neutral ialah 7.
- Semakin tinggi kepekatan ion hidroksida dalam suatu larutan Semakin besar nilai pH larutan alkali itu.
- Nilai pH larutan alkali adalah lebih daripada 7. Semakin besar nilai pH larutan semakin tinggi kealkaliannya.
Penunjuk Asid dan Alkali
- Penunjuk asid dan alkali ialah sejenis bahan kimia apabila ditambah ke dalam larutan berasid atau beralkali akan memberi warna yang berbeza pada nilai pH yang berbeza.
- Jadual di bawah menunjukkan warna-warna bagi penunjuk-penunjuk tertentu di dalam larutan neutral , larutan berasid atau larutan beralkali.PenunjukWarna dalam asid pH<7Warna semasa neutral pH=7Warna dalam alkali pH >7litmusmerahungubirufenolftaleintidak berwarnatidak berwarnamerah jambumetil jinggamerah jambujingga pada pH 6kuningmetil merahmerahjinggakuningbromotimol birukuninghijaubiru
 |
| (Warna penunjuk universal pada pH yang berlainan) |
| (Kertas litmus. Warnanya biru dalam alkali dan merah di dalam asid) |
 |
| (Warna fenolftalein dalam alkali) |
(Metil jingga: Kiri: Asid; Kanan: Alkali. This image is shared by Rubashkyn in wikipedia) |
 |
| (Metil merah: Kiri: Asid; Kanan: Alkali. This image is shared by LHcheM in Wikipedia) |
 |
| (Bromotimol biru. Kiri: Asid; Kanan: Alkali).) |
 |
| (Penunjuk universal. This image is shared by Bordercolliez in wikipedia) |