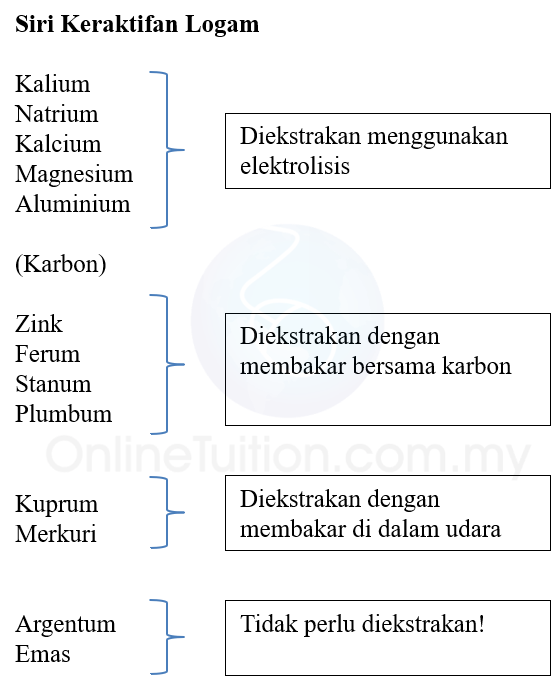
Jika kepekatan sesuatu ion itu sangat tinggi, maka ion itu akan dipilih untuk nyacas, walaupun ia terletak di bahagian yang lebih tinggi di dalam siri elektrokimia.
Elektrolisis Asid Hidroklorik Cair
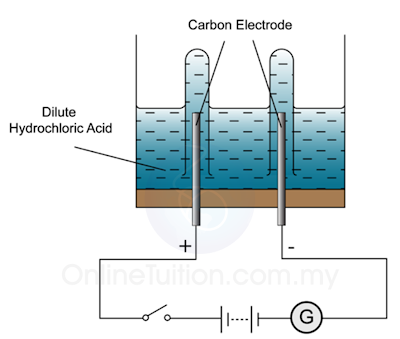
Ion-ion yang hadir di
Anod:
Cl–, OH–
Katod:
H+
Pemerhatian dan Kesimpulan
Anod:
Pemerhatian: Gelembung gas tak berwarna dan tak berbau dibebaskan. Gas ini menyalakan kayu uji berbara.
Kesimpulan: Gas oksigen dihasilkan
Katod:
Pemerhatian: Gelembung gas tak berwarna dan tak berbau dibebaskan. Apabila kayu uji bernyala diletakkan pada mulut tabung uji, bunyi `pop’ terhasil.
Kesimpulan: Gas hidrogen dihasilkan
Persamaan separa bagi tindakbalas di
Anod:
4OH– → 2H2O + O2 + 4e
Katod:
H+ + 2e → H2
Elektrolisis Asid Hidroklorik Pekat
Ion-ion yang hadir di
Anod:
Cl–, OH–
Katod:
H+
Pemerhatian dan Kesimpulan
Anod:
Pemerhatian:
Gas berwarna kuning kehijauan dihasilkan. Jika kertas litmus biru lembap dimasukkan ke dalam tabung uji yang mengandungi gas ini, kertas litmus merah lembap bertukar memjadi merah, seterusnya warnanya dilunturkan.
Kesimpulan: Gas klorin dihasilkan
Katod
Gelembung gas tak berwarna dan tak berbau dibebaskan. Apabila kayu uji bernyala diletakkan pada mulut tabung uji, bunyi `pop’ terhasil.
Kesimpulan:
Gas hidrogen dihasilkan
Persamaan separa bagi tindakbalas di
Anod:
2Cl– → Cl + 2e
Katod:
H+ + 2e → H2