- Siri elektrokimia ialah satu siri susunan logam mengikut susunan kecenderungan logam untuk kehilangan elektron membentuk ion positif.
- Unsur-unsur yang diletak lebih tinggi dalam siri elektrokimia
- lebih elektropositif
- bertindak sebagai agen penurunan yang kuat
- boleh dioksidakan dengan mudah
- Ion logam ialah agen pengoksidaan yang lemah kerana mereka tidak mempunyai kecenderungan untuk mendapatkan elektron.
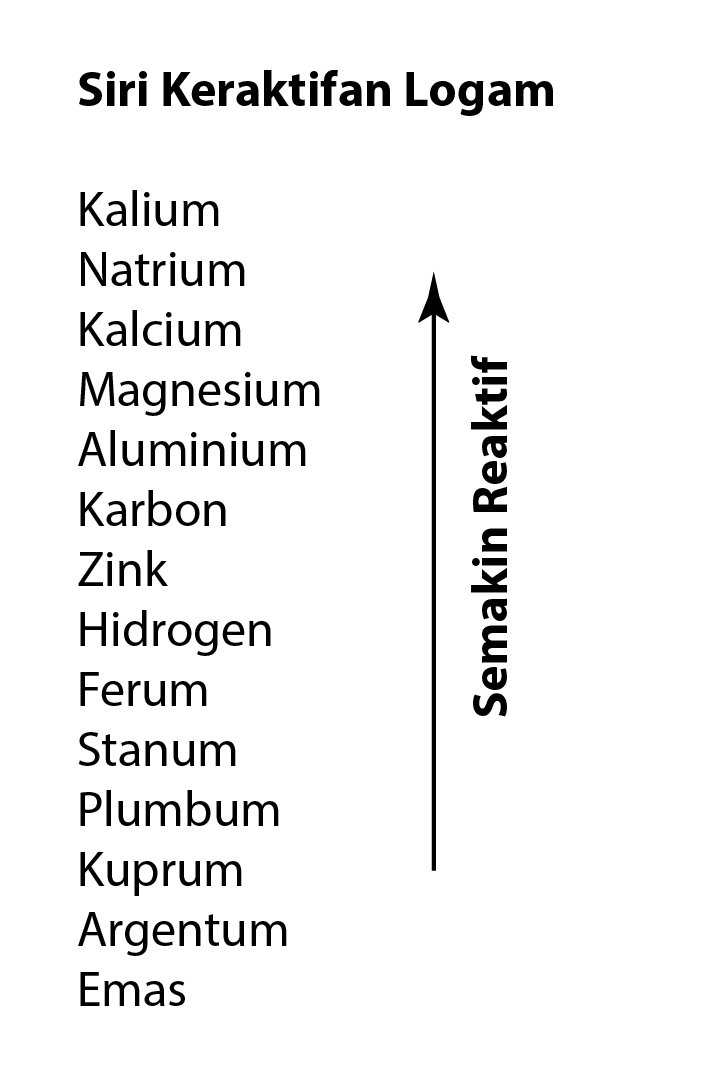
- Dalam tindak balas penyesaran logam, logam yang diletakkan di bahagian atas siri elektrokimia (lebih elektropositif) boleh menggantikan logam lain yang terletak di bawahnya (kurang elektropositif) daripada larutan garamnya.
- Oleh itu,
- terdapat pemindahan elektron daripada logam yang lebih elektropositif kepada ion logam yang kurang elektropositif.
- logam yang lebih elektropositif bertindak sebagai agen penurunan. Logam yang mengalami pengoksidaan dioksidakan menjadi ion logam.
- ion logam yang kurang elektropositif bertindak sebagai agen pengoksidaan. Ion-ion logam ini mengalami penurunan dan diturunkan menjadi atom logam.
Contoh
Tindak balas di antara larutan magnesium dan kuprum(II) sulfat
Mg + CuSO4 → MgSO4 + Cu
Pemerhatian:
Warna biru larutan kuprum(II) sulfat berubah menjadi tidak berwarna.
Persamaan setengah:
Mg → Mg2+ + 2e
Cu2+ + 2e → Cu
Persamaan ion:
Mg + Cu2+ → Mg2+ + Cu
Nota:
- Magnesium lebih elektropositif daripada kuprum.
- Dalam tindak balas, magnesium menyesarkan ion kuprum(II) dari larutannya.
- Magnesium dioksidakan dengan melepaskan 2 elektron.
- Ion kuprum(II) diturunkan dengan menerima 2 elektron daripada magnesium.
Agen pengoksidaan: Ion kuprum(II)
Agen penurunan: Magnesium