Hukum Charles menyatakan bahawa bagi suatu gas yang jisimnya tetap, isi padunya berkadar langsung kepada suhu mutlaknya jika tekanan gas adalah malar, iaitu
Formula:
Penerangan
- Pada tekanan yang tetap, kekerapan perlanggaran antara molekul gas dengan dinding bekas adalah malar.
- Jika suhu gas bertambah, tenaga kinetik molekul molekul juga bertambah.
- Ini menambahkan kekerapan perlanggaran antara molekul gas dengan dinding bekas, maka tekanan gas sepatutnya bertambah.
- Untuk mengekalkan tekanan gas pada nilai malarnya, bilangan molekul gas per unit isipadu perlu dikurangkan, maka isi padu gas bertambah.
- Kesimpulannya ialah isipadu gas bertambah apabila suhu gas bertambah.
Graf
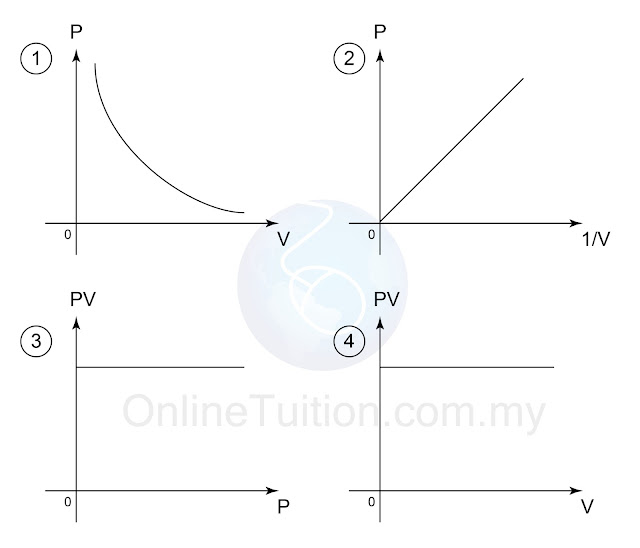
- Graf 1 menunjukkan bahawa isi padu gas V adalah berkadar langsung dengan suhu mutlak.
- Graf 2 menunjukkan bahawa jika suhu adalam dalam unit °C, garis lurus itu tidak melalui asalan.
- Graf 3 dan 4 menunjukkan bahawa V/T adalah malar bagi sebarang nilai V dan T.