| Tindak Balas Kimia | Mangkin |
|---|
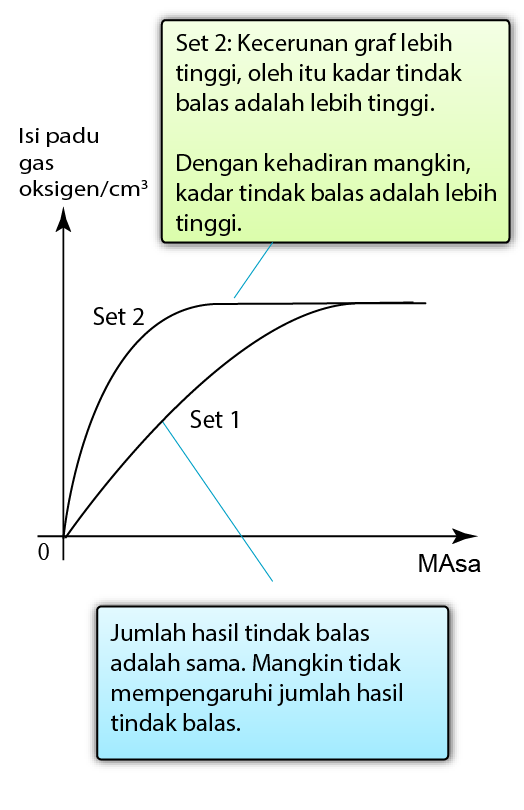
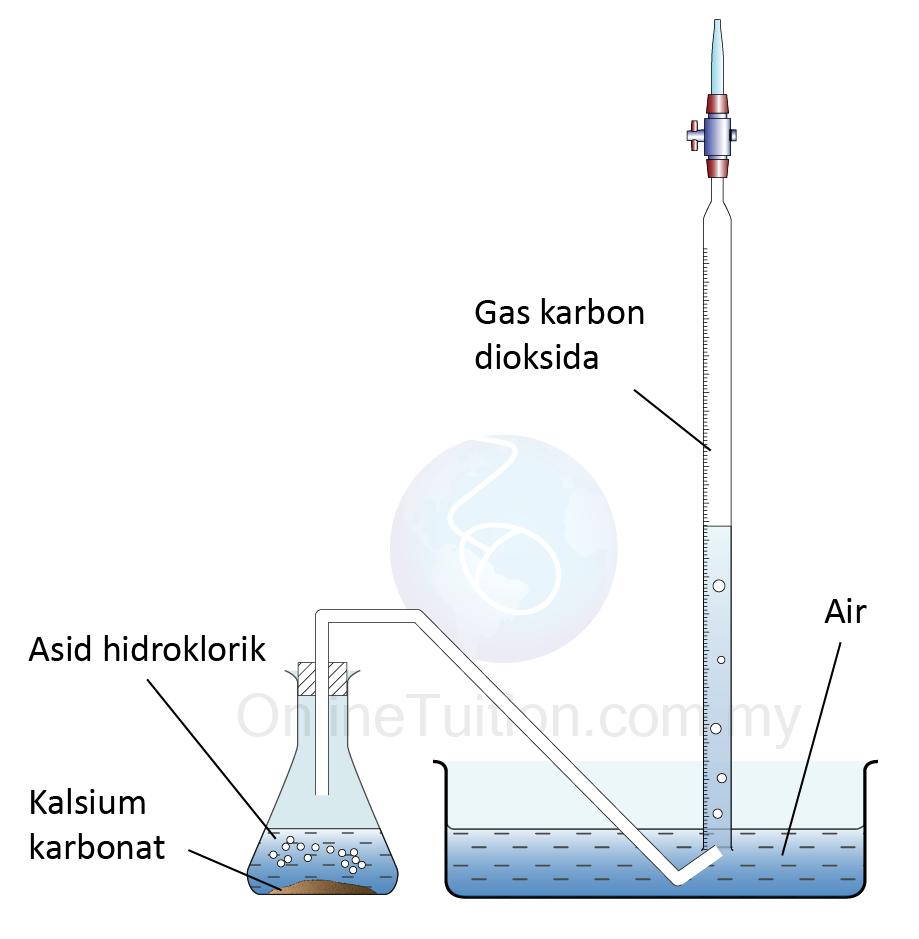
Penguraian hidrogen peroksida:
2H2O2 → 2H2O + O2 | Mangan(IV) oksida, MnO2
Plumbum(II) oksida, PbO
Plumbum(IV) oksida, PbO2 |
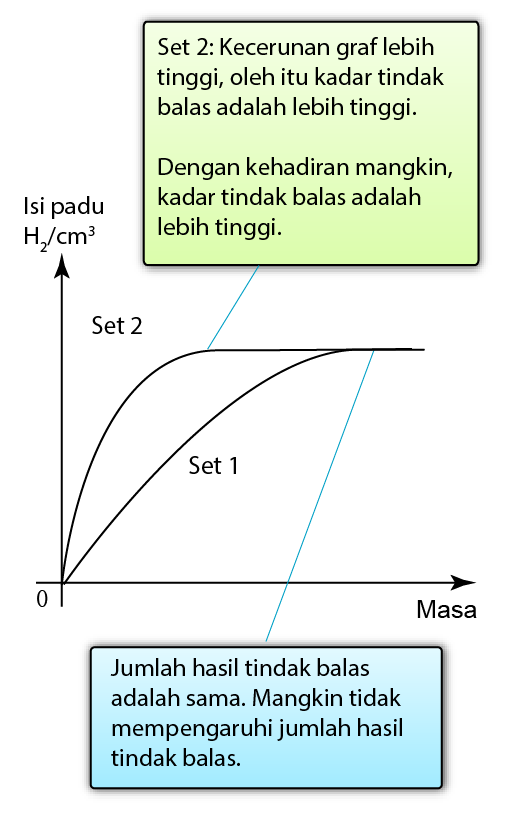
Tindak balas antara zink dan asid hidroklorik:
Zn + 2HCl → ZnCl2 + H2 | Manganese (IV) oksida, MnO2
Kuprum(II) oksida, CuO
Zink Oxide, ZnO
Silikon(IV) oksida, SiO2 |
Penguraian Kalium Klorat(V):
2KClO3 + 2KCl → 3O2 | Kuprum(II) sulfat, CuSO4
Kuprum(II) klorida, CuCl2
Kuprum(II) nitrat, Cu(NO3)2 |
Proses Haber
N2 + 3H2 → 2NH3 | Ferum |
Proses Sentuh
2SO2 + O2 → 2SO3 | Vanadium(V) oksida, V2O5 |
Proses Ostwald
4NH3(g) + 5O2(g) 4NO(g) + 6H2O(1) | Platinum |